The Conversation
Production renouvelable d’hydrogène par les microalgues : révolution ou utopie ?Production renouvelable d’hydrogène par les microalgues : révolution ou utopie ?

Après l’ère des combustibles fossiles (pétrole et gaz naturel) qui génèrent de nombreux problèmes environnementaux, la période à venir sera-t-elle celle de l’hydrogène ? Son intérêt réside dans sa capacité à produire de l’électricité, de l’eau et de la chaleur lorsqu’il se combine à l’oxygène dans une pile à combustible : un dispositif reposant sur l’oxydation de l’hydrogène et la réduction de l’oxygène au niveau de deux électrodes, le déplacement des électrons entre celles-ci génère de l’électricité.
 Culture de microalgues. CSIRO, CC BY-SA
Culture de microalgues. CSIRO, CC BY-SA
L’hydrogène peut facilement être obtenu par électrolyse de l’eau (séparation de ses deux composants dioxygène et dihydrogène grâce à un courant électrique) mais cette méthode n’est pas encore économiquement très rentable, car elle consomme beaucoup d’électricité à prix élevé que l’on doit produire par ailleurs ; un couplage avec des éoliennes pourrait être une solution. Actuellement, l’hydrogène est principalement produit à partir de composés organiques comme le gaz naturel par reformage (réaction chimique au cours de laquelle la chaleur casse les molécules carbonées pour en libérer l’hydrogène), le charbon par gazéification (transformation thermique et chimique d’un solide en gaz) ou la biomasse par fermentation, ces procédés rejetant beaucoup de CO2.
Comment faire ?
Les plantes savent dissocier les deux composants de l’eau. Un vieux projet de production d’hydrogène revient sur le devant de la scène : il s’inspire de la photosynthèse qui se déroule en permanence à la lumière dans les feuilles des plantes.
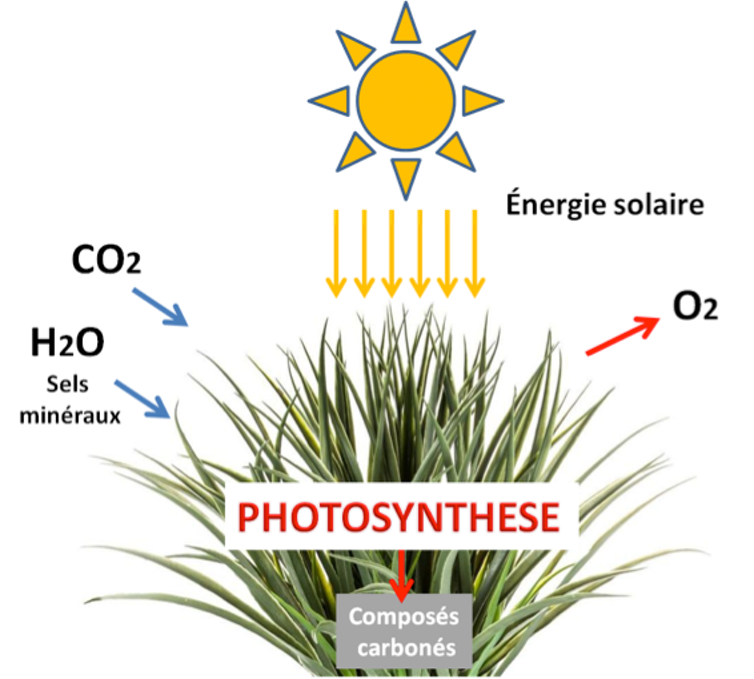 Schéma de fonctionnement de la photosynthèse. G. Tremblin, B. Veidl, Author provided
Schéma de fonctionnement de la photosynthèse. G. Tremblin, B. Veidl, Author provided
La photosynthèse entraîne la scission de l’eau H2O en ses deux composants : le dioxygène O2 et les deux protons H+ : C’est la photolyse. Chez les plantes, le pouvoir réducteur des protons permet d’activer la voie de synthèse de composés organiques principalement l’amidon.
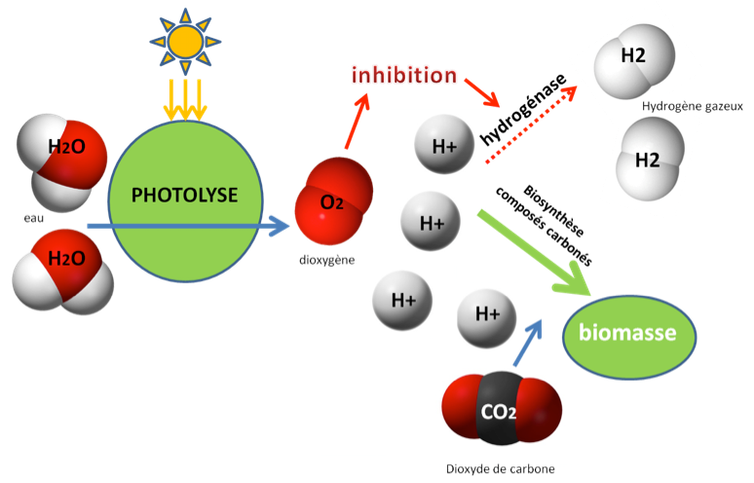 Schéma de la production d’hydrogène par photolyse. G. Tremblin, B. Veidl, Author provided
Schéma de la production d’hydrogène par photolyse. G. Tremblin, B. Veidl, Author provided
La stratégie est donc de récupérer ces protons H+ sous forme d’hydrogène moléculaire H2 avant qu’ils ne soient utilisés dans la chaîne photosynthétique des cellules pour produire de la biomasse. On peut alors imaginer des cellules végétales capables de produire de l’hydrogène à partir seulement d’eau et de soleil !
Heureusement, il y a les microalgues !
Dès 1940, la capacité de microalgues à produire de l’hydrogène dans certaines conditions a été mise en évidence. Cependant, c’est beaucoup plus tard à la fin du vingtième siècle qu’un certain Anastasios Melis, chercheur a l’université de Californie, a expliqué pourquoi ce mécanisme était éphémère : l’enzyme responsable de la conversion des protons H+ en hydrogène appelée hydrogénase, est inhibée par le dioxygène produit par la photosynthèse. Un inhibiteur enzymatique est une substance qui, en se liant à une enzyme en diminue l’activité, soit en se fixant sur le site actif, soit en provoquant une déformation de la protéine enzymatique la rendant inactive.
Comment résoudre ce problème d’inhibition ? Plusieurs démarches sont entreprises par les équipes de recherche engagées sur cette thématique :
La première approche consiste à rendre les hydrogénases insensibles au dioxygène. Une autre démarche se base sur la flexibilité métabolique des microalgues qui présentent, dans certaines conditions, en particulier lorsqu’on les carence en soufre, une capacité à orienter leur métabolisme photosynthétique vers la production d’hydrogène.
Par ailleurs, il a récemment été montré que des microalgues encapsulées dans des gouttelettes étaient capables de produire de l’hydrogène en absence d’oxygène. Toutefois, la stabilité de ces microréacteurs reste limitée à quelques jours de fonctionnement. Deux équipes de Le Mans Université, le Laboratoire « Mer Molécules Santé » (MMS) et l’Institut des Molécules et Matériaux du Mans (IMMM) ont initié un travail visant à encapsuler des microalgues et des cyanobactéries (bactéries photosynthétiques, les plus connues étant les spirulines, voir notre article paru dans The Conversation) dans des hydrogels en vue de créer des microbioréacteurs solides capables de produire de l’hydrogène sur une longue période.
D’autre part, les spécialistes des photo-bioréacteurs (dispositifs permettant de cultiver à la lumière des microorganismes photosynthétiques dans un milieu de culture) du GEPEA (Laboratoire de Génie des procédés pour les écotechnologies et les bioressources) travaillent actuellement sur un processus en deux étapes. Lors de la première étape, les microalgues sont cultivées dans un milieu de culture carencé en azote et produisent de la biomasse riche en amidon. La seconde étape favorise la production de l’hydrogène par les microalgues grâce à une anoxie obtenue en réduisant l’éclairement ce qui favorise la respiration (consommatrice d’oxygène) au détriment de la photosynthèse.
En Israël, une équipe de chercheurs a réussi à sélectionner des mutants de microalgues dont l’activité photosynthétique est complètement inhibée à une température de 37 °C. Ils ont conçu le dispositif présenté ci-dessous.
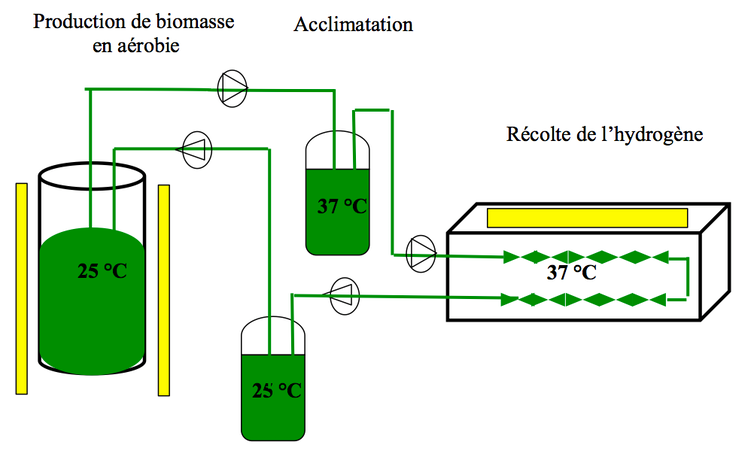 Schéma de production d’hydrogène à partir de microalgues. G. Tremblin, B. Veidl, Author provided
Schéma de production d’hydrogène à partir de microalgues. G. Tremblin, B. Veidl, Author provided
Ce photobioréacteur est dit cyclique. Dans une première phase, les microalgues sont cultivées à 25 °C, à la lumière, dans un milieu carencé en soufre et en azote afin de favoriser la synthèse d’amidon et le fonctionnement de l’hydrogénase.
Elles sont ensuite transférées dans une autre enceinte à 37 °C, la seconde phase commence alors : la photosynthèse de ces microalgues modifiées s’arrête et le milieu devient anoxique ce qui initie la production d’hydrogène.
L’hydrogène est récupéré par diffusion et les microalgues sont ensuite réorientées vers la phase de production de biomasse. Un autre cycle peut alors démarrer.
Pour l’instant, quel que soit le dispositif utilisé, le rendement de production d’hydrogène par des microalgues reste malgré tout assez faible.
Quelles sont les microalgues candidates ?
Une microalgue verte, Chlamydomonas reinharditii a été retenue comme modèle dans de nombreuses expérimentations car elle possède au niveau de sa chaîne photosynthétique une hydrogénase à fer très active.
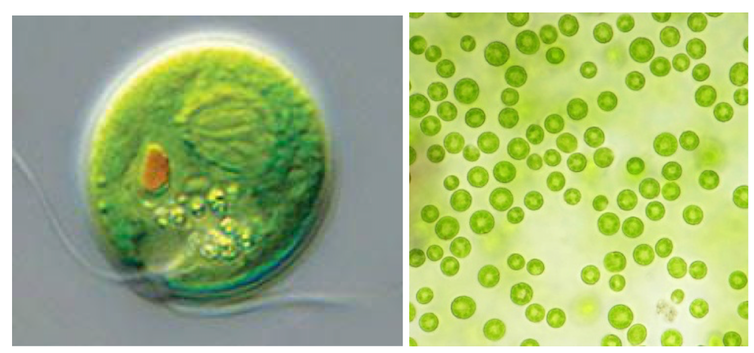 Chlamydomonas reinharditii vue en microcopie optique. G. Tremblin, B. Veidl, Author provided
Chlamydomonas reinharditii vue en microcopie optique. G. Tremblin, B. Veidl, Author provided
La chlorelle, microalgue verte unicellulaire (Chlorella vulgaris) et la cyanobactérie filamenteuse du genre Anabaena ont été retenues par l’équipe du Mans, car ce sont des modèles dont les caractéristiques sont bien connues et la culture bien maîtrisée au niveau du laboratoire.
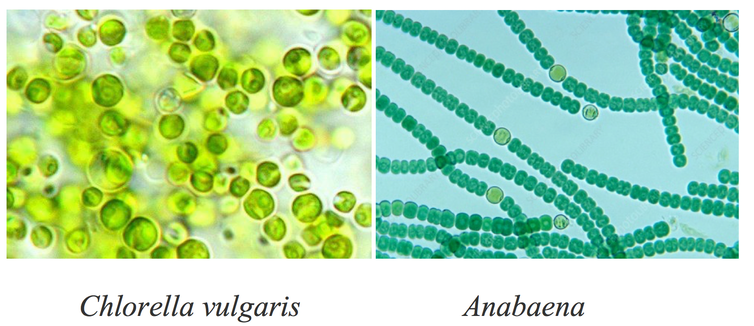 Observations de Chlorella vulgaris et de la cyanobactérie du genre Anabaena. G. Tremblin, B. Veidl, Author provided
Observations de Chlorella vulgaris et de la cyanobactérie du genre Anabaena. G. Tremblin, B. Veidl, Author provided
L’hydrogène est maintenant considéré comme une source d’énergie d’avenir non polluante et renouvelable : son utilisation dans les véhicules ne produit pas de CO2 et l’eau formée dans cette réaction retourne dans la biosphère.
Lorsque les chercheurs auront réussi à obtenir une microalgue possédant une hydrogénase capable de fonctionner sans être inhibée par le dioxygène et avec un rendement suffisant pour produire de l’hydrogène, un processus industriel pourra être développé. Les verrous sont encore nombreux mais les scientifiques s’ingénient à les faire sauter les uns après les autres et dans un avenir que l’on n’espère pas trop lointain, des dispositifs de production à grande échelle pourront voir le jour.
Ils pourraient prendre l’aspect d’immenses bassins ou mieux de grands photobioréacteurs installés dans des zones désertiques qui permettront de produire de façon renouvelable les énormes quantités de bio hydrogène ou hydrogène vert dont le monde a tant besoin, en n’utilisant que du soleil et de l’eau.
Cet article a été écrit avec l'appui de Caroline Gilbert, présidente du groupe de travail Anses « évaluation du risque de morsure par les chiens » et Florence Étoré Adjointe, chef d’unité à l'Anses Direction de l’évaluation des risques (DER).
Auteurs :
Gérard Tremblin, enseignant-chercheur en biologie végétale à Le Mans Université, laboratoire Mer, Molécules, Santé (MMS - EA 2160), et Brigitte Veidl ingénieure d'études à Le Mans Université.
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.
